Điều trị nhiễm Helicobacter pylori trong tình hình kháng thuốc hiện nay
Lịch sử quá trình phát hiện và điều trị vi khuẩn Hp (H.pylori)
Trong thập niên 1970, “no acid, no ulcer” (không acid, không loét), câu nói lừng danh của Carl Schwarz (1868-1917), một thầy thuốc ngoại khoa người Nam Tư đã thống lĩnh trong nhiều sách giáo khoa y học về tiêu hoá trong hơn 50 năm. Theo đó, bệnh loét dạ dày-tá tràng được xem là hậu quả của tác động của acid trên niêm mạc dạ dày.
Tuy nhiên, với những hiểu biết mới về vi trùng Helicobacter pylori, cơ chế bệnh sinh của bệnh LDDTT đã được định nghĩa lại, từ một bệnh do acid sang một bệnh do nhiễm trùng. Nhiễm trùng H. pylori được xem là nguyên nhân của loét dạ dày tá tràng, ung thư dạ dày và MALT. Từ đó, quan điểm điều trị đã thay đổi sâu sắc: từ chỗ chỉ trung hoà acid dạ dày, tiến đến điều trị tiêu diệt vi trùng bằng cách kết hợp kháng sinh với các thuốc ức chế bơm proton (PPI).
Gần 20 năm sau khi thiết lập được chế độ điều trị 3 thuốc có clarithromycine để tiêu diệt Helicobacter pylori [Bazzoli et al. 1993; Lamouliatte et al. 1993], hiệu quả của phác đồ này đã nhanh chóng giảm đi ở mức độ toàn cầu. Mục tiêu điều trị để đạt được tỷ lệ làm sạch vi trùng ít nhất là 80% nhiều khi không đạt được, làm cho việc tái điều trị ngày càng thường xuyên hơn trong thực hành lâm sàng.
Một trong những nguyên nhân thất bại điều trị ngày càng được thấy rõ là sự gia tăng đề kháng với clarithromycine [Megraud và Lamouliatte 2003]. Khi levofloxacine được sử dụng để thay thế clarithromycine [Cammarota et al. 2000], nó cũng bị đề kháng nhanh chóng. Có nhiều cách để vượt qua sự đề kháng này, trong đó có phương pháp kết hợp nhiều thuốc chưa bị kháng nhiều. Phác đồ điều trị 4 thuốc với PPI, bismuth subcitrate potassium, metronidazole, và tetracycline là phác đồ phổ biến, tuy có nhiều tác dụng phụ khó chịu cho người bệnh. Một trong những hướng đi đầy hứa hẹn trong tương lai là kết hợp thêm kháng thể đặc hiệu từ lòng đỏ trứng (IgY-Hp).
Gia tăng đề kháng của Hp với Clarithromycine và Levofloxacine
Đột biến là cơ chế kháng thuốc của H. pylori . Trong trường hợp clarithromycine, có 3 điểm đột biến kháng thuốc ở 2 vị trí 2142 (A2142G và A2142C) và 2143 (A2143G) tại quai peptidyl transferase của gene 23S rRNA; những đột biến này làm giảm gắn kết với thuốc, có thể xảy ra ngẫu nhiên và tồn tại qua nhiều thế hệ vi trùng. Hơn nữa, mọi macrolides đều có cơ chế đột biến tương tự [Megraud and Lehours, 2007]. Thường thì vi trùng đột biến kháng clarithromycine chỉ chiếm một tỷ lệ nhỏ trong quần thể H. pylori. Tuy nhiên, khi tần suất kê toa tăng lên, những dòng đột biến này sẽ được chọn lọc và trở thành đa số trong quần thể vi trùng.
Ở Việt nam, theo nghiên cứu của Nguyễn Thuý Vinh và cộng sự năm 2004 tại Hà nội, tỷ lệ H. pylori kháng clarithromycine là 5.5%. Trong khi đó, tỷ lệ kháng clarythromycine ở khu vực Sài gòn là 38.5% (Lê Đình Minh Nhân và cộng sự, 2006).
Ở Hoa kỳ, tỷ lệ kháng clarythromycine là 10% trong giai đoạn 1994-2000, Trong khi tỷ lệ này là 21% ở châu Âu từ 2008-2009. Tỷ lệ kháng clarithromycine đã được chứng minh là một yếu tố nguy cơ độc lập làm điều trị thất bại (p = 0.004) cũng như độ tiến triển từ khó tiêu không loét sang loét dạ dày (p = 0.003) trong một nghiên cứu đa biến [Moayyedi et al. 2011].
Kháng clarithromycine là yếu tố tiên đoán mạnh nhất của thất bại điều trị. Khi tỉ lệ kháng clarithromycine trong quần thể 10-15%, tỉ lệ tiệt trừ thành công của liệu pháp 3 thuốc chứa clarithromycine giảm xuống dưới mức khuyến nghị là 80%. Thậm chí tiệt trừ thành công thấp chỉ đạt 40-75% đã được báo cáo ở nhiều nước như Ý, Thổ nhĩ kỳ, Pháp, Bỉ, Brazil, Nam phi, Nhật, Trung quốc(Altintas 2004,Perri F 2001, Bigard MA 1998, Eclissato C2002, Lee JM 1999, Wong BCY 2000). Do đó, ở những vùng gia tăng tỉ lệ kháng clarithromycine ( >15-20%), hoặc khi bệnh nhân trước đó đã dùng macrolide, không nên dùng liệu pháp 3 thuốc có chứa clarithromycine để điều trị nhiễm H. pylori.
Điều tương tự cũng xảy ra với levofloxacine và tất cả fluoroquinolones, ngoại trừ đột biến xảy ra ở vị trí khác, DNA gyrase và ở mức độ phổ biến hơn kháng macrolides. Đột biến này làm giảm độ ức chế sự nhân đôi nhiễm sắc thể vi trùng của thuốc [Megraud and Lehours, 2007].
Đề kháng kháng sinh do đột biến thường gia tăng chậm nhưng tiến triển trong trường hợp H. pylori kháng với clarithromycine và levofloxacine. Trên thế giới, tỷ lệ kháng clarythromycine đã đạt tới 20% hay hơn [Megraud et al. 2011], và là nguyên nhân chính làm thất bại điều trị. 10 năm sau khi xuất hiện kháng clarythromycine, tình trạng kháng levofloxacine tái diễn, đến mức nhiều quốc gia đã không cho phép sử dụng levofloxacine để điều trị mù (empiric) khi chưa có kháng sinh đồ.
Tác động của kháng clarithromycine trên tỷ lệ tiệt trừ H. pylori được chứng minh trong nhiều nghiên cứu có thử nghiệm kháng sinh đồ. Trong một tổng phân tích của Fischbachand, mức độ thành công của điều trị 3 thuốc, giảm xuống còn 66.2% khi H. pylori kháng với clarithromycine. Kết quả tương tự cũng được ghi nhận với kháng levofloxacine [Perna et al. 2007].
Điều chỉnh phác đồ điều trị ở những vùng có tỷ lệ kháng thuốc cao
Điều trị theo từng cá thể (Tailored treatment)
Đây là một cách hợp lý khi có thể thử nghiệm mức độ nhạy cảm với kháng sinh của H. pylori. Ngay cả khi tỷ lệ kháng clarithormycine lên đến 25-30%, những bệnh nhân không kháng thuốc còn lại vẫn có thể được điều trị khỏi với phác đồ 3 thuốc. Phương pháp tiêu chuẩn là cấy và làm kháng sinh đồ (Etest, AB bioMerieux, Solna, Sweden) cần nhiều ngày mới có kết quả. Phương pháp thử nhanh bằng sinh học phân tử có thể phát hiện cả H. pylori và đề kháng macrolides. Chúng gồm các phương pháp PCR tiêu chuẩn (Seeflex®ClaR H. pylori ACE detection, Seegene, Seoul, South Korea) [Lehours et al. 2011], PCR theo thời gian thực (Engenetix, Vienna, Austria) [Schabereiter-Gurtner et al. 2004], hay lai hoá huỳnh quang tại chỗ (fluorescence in situ hybridization (seaFAST H. pylori , SeaPro Theranostics International, Lelystad, The Netherlands) [Russmann et al. 2001]. Những phương pháp này không đòi hỏi vận chuyển đặc biệt, dễ thực hiện, tin cậy và nhanh chóng. Người ta cũng áp dụng phương pháp sinh học phân tử để phát hiện kháng levofloxacine (HelicoDR, Hain LifeScience, Nehren, Germany) [Cambau et al. 2009].
Tuy nhiên, phương pháp thử nghiệm độ nhạy thuốc vẫn có những giới hạn. Không ít toa thuốc tiệt trừ H. pylori là sau một khảo sát không xâm lấn nên không có bệnh phẩm. Và đến nay, nhiều thầy thuốc tiêu hoá vẫn chưa có khảo sát một cách thường qui độ nhạy thuốc của H. pylori trước khi điều trị.
Điều trị tiếp nối (sequential treatment)
Có thể giảm thiểu kháng thuốc khi kê toa kháng sinh tuần tự thay vì cùng một lần. Zullo và cộng sự đề xuất sử dụng PPI với amoxicillin trong 5 ngày đầu, theo sau là PPI với clarithromycine và metronidazole trong 5 ngày tiếp. [Zullo et al. 2000]; Phác đồ này có hiệu quả để tiêu diệt những dòng H. pylori kháng clarithromycine, làm tăng tỷ lệ thành công lên 72% so với điều trị tiêu chuẩn là 33% khi có kháng clarythromycine [Gisbert et al. 2010].
Cơ chế giải thích cho cách điều trị tuần tự này là cho amoxcilline trước để giảm tải vi trùng, tiêu diệt hầu hết hoặc tất cả những vi trùng kháng clarythromycine. Giai đoạn 2 tiêu diệt những vi trùng còn lại mà không kháng clarythromycine.
Người ta đã nghiên cứu nhiều phác đồ điều trị tuần tự, thay đổi thời gian điều trị từ 4-7 ngày cho mỗi giai đoạn và/hoặc thuốc được sử dụng. Phác đồ điều trị tuần tự với levofloxacine cũng đạt được thành công 82.5% ở Tây ban nha [Molina-Infante et al. 2010] và 96% ở Ý [Romano et al. 2010].

Phác đồ điều trị 4 thuốc có Bismuth
Mục đích của phác đồ này là tránh sử dụng những kháng sinh đã bị đề kháng, clarithromycine và levofloxacine. Ngay sau khi phát hiện ra H. pylori, Marshall và cộng sự đã điểm lại những y văn trước đó cho thấy nhiều hoạt chất có tính kháng sinh như muối bismuth và metronidazole đã được sử dụng để điều trị loét dạ dày trong quá khứ với những thành công nhất định.Tác giả đã phối hợp hai thành phần trên để so sánh mù đôi với cimetidine, và ghi nhận đã tiệt trừ được H. pylori trong hầu hết các trường hợp với tỷ lệ tái phát loét tá tràng rất thấp sau 1 năm ở những người sử dụng phối hợp kháng sinh. [Marshall et al. 1988].
Năm 1987, Borody đã tiệt trừ thành công H. pylori bằng kết hợp muối bismuth, metronidazole và tetracycline [Borody et al. 1987]. Phác đồ này đã được chính thức khuyến nghị tại Hội nghị tiêu hoá Thế giới tại Sidney, Úc năm 1990 [Tytgat et al. 1990], và sau đó là đồng thuận của Viện Sức khoẻ Quốc gia Hoa Kỳ năm 1994 [NIH, 1994]. Một tổng quan của Penston năm 1994 gồm 67 nghiên cứu và 2787 bệnh nhân cho thấy tỷ lệ tiệt trừ vi trùng là 72% [Penston, 1994]. Năm 1995, có hai nghiên cứu độc lập cho thấy bổ sung PPI vào phác đồ 3 thuốc có bismuth làm tăng tỷ lệ lành bệnh [de Boer et al. 1995; Borody et al. 1995].
Cơ chế tác động của phác đồ 4 thuốc có thể kể ra như sau
- Muối Bismuth có tác dụng ngắn hạn tại chỗ; cơ chế tác dụng thì chưa rõ nhưng dường như nó có tác dụng sát trung hơn là diệt khuẩn. Và không ghi nhận kháng thuốc.
- Tetracycline là một kháng sinh rất hiếm khi bị đề kháng vì phải cần 3 điểm đột biến kế cận nhau mới xuất hiện kháng thuốc. Xác suất này rất thấp.
- Với Metronidazole, đề kháng in vitro xuất hiện với tần số cao trong hầu hết các quốc gia, nhưng không quan trọng về lâm sàng và có thể vượt qua bằng cách tăng liều và thời gian điều trị. Tổng phân tích của Fischbach và Evans ghi nhận thành công về mặt lâm sàng sẽ giảm đi 14% khi có kháng thuốc in vitro [Fischbach và Evans, 2007].
Tuy vậy, tỷ lệ thành công của phác đồ 4 thuốc có bismuth trên 9 nghiên cứu ở 1674 bệnh nhân cũng chỉ vào khoảng 78%, tương đương với tỷ lệ 77% ở những phác đồ thay thế khác và không khác biệt có ý nghĩa [Luther et al. 2010].
Dù có nhiều lợi điểm về mặt tiệt trừ vi khuẩn, không thể không kể đến những tác dụng phụ đáng kể của phác đồ 4 thuốc có bismuth. Tuy bismuth không hấp thu qua vào máu (<1%), sử dụng liều cao và kéo dài có thể làm tăng nồng độ bismuth trong máu. Năm 1987, ở Pháp đã ghi nhận muối bismuth liều cao liên quan đến bệnh não và có thể gây tử vong, làm cho giới chức y tế cấm sử dụng bismuth [Bader, 1987]. Bên cạnh đó, những tác dụng phụ, đặc biệt trên đường tiêu hoá của tetracycline và metronidazole cũng chiếm một tỷ lệ đáng kể trên thực tế lâm sàng
Khuyến nghị thực hành theo Hội nghị đồng thuận về chẩn đoán và điều trị Hp ở Việt Nam (Hội Khoa học Tiêu hoá Việt Nam,2012)
Chỉ định điều trị tiệt trừ H. pylori:
- Rối loạn tiêu hóa (dyspepsia)
- Tiền sử loét DD-TT chưa biết tình trạng nhiễm HP
- Viêm / loét DD – TT trên nội soi
- Có cha mẹ hoặc anh chị em ruột bị UTDD
- Sau phẫu thuật UTDD
- Cần điều trị lâu dài với NSAIDs
- Cần điều trị ASA lâu dài ở BN nguy cơ cao, bị loét/biến chứng của loét DD – TT
- GERD cần điều trị duy trì lâu dài bằng PPI
- Thiếu máu thiếu sắt không rõ nguyên nhân
- Ban xuất huyết giảm tiểu cầu vô căn
- BN muốn được điều trị (sau khi đã được BS tư vấn)
Các phác đồ điều trị tiệt trừ Helicobacter pylori

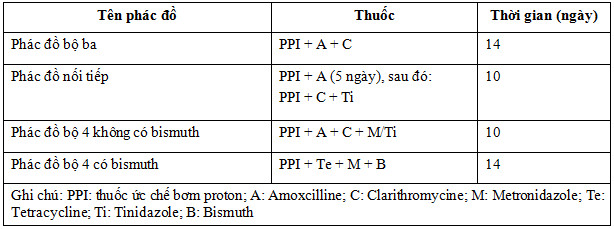 Liều thuốc sử dụng trong các phác đồ điều trị tiệt trừ H. pylori
Liều thuốc sử dụng trong các phác đồ điều trị tiệt trừ H. pylori
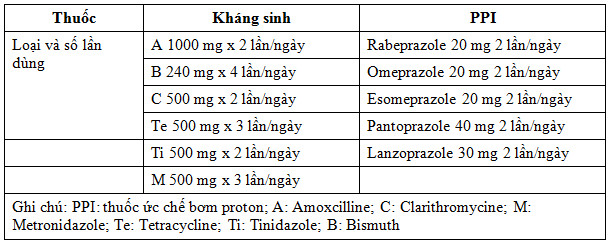
Tại miền Trung và Bắc, vì tỷ lệ kháng Clarythromycine không quá cao, có thể sử dụng phác đồ PPI + A + C trong 10-14 ngày. Ngược lại, ở miền Nam vì tỷ lệ kháng thuốc cao, tỷ lệ thành công của phác đồ có Clarythromycine chỉ khoảng 70% hay thấp hơn,nên sử dụng phác đồ nối tiếp hoặc phác đồ 4 thuốc (có / không có Bismuth) sử dụng đồng thời.
Kết quả phác đồ đầu tay điều trị tiệt trừ H.Pylori ở Việt Nam
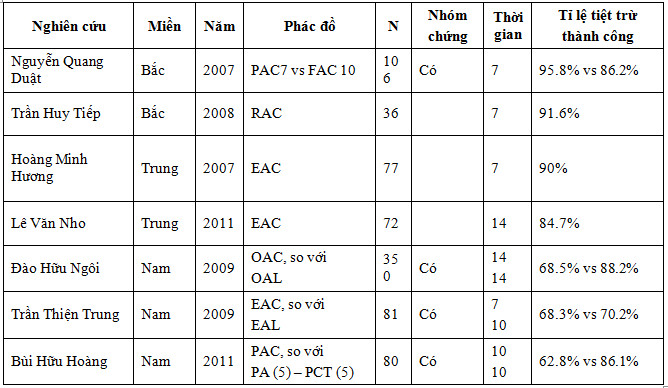
Phác đồ tiệt trừ Helicobacter pylori lần 2:
Sử dụng phác đồ 4 thuốc có Bismuth nếu trước đó chưa dùng
Sử dụng phác đồ PPI+A+L nếu trước đã dùng phác đồ 4 thuốc có Bismuth thất bại.
Kết quả phác đồ thứ 2 trong điều trị tiệt trừ H. pylori ở Việt Nam
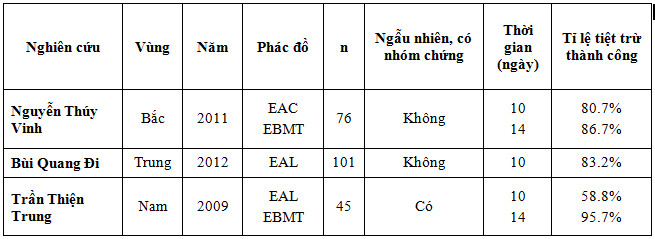
Không dùng lại kháng sinh đã sử dụng trong phác đồ điều trị bị thất bại trước đó, đặc biệt là Clarithromycine (ngoại trừ Amoxicilline) vì tỉ lệ kháng thứ phát rất cao
Phác đồ điều trị cứu vãn:
Trong trường hợp vẫn diệt trừ thất bại sau hai lần điều trị, cần nuôi cấy vi khuẩn và làm kháng sinh đồ để chọn kháng sinh phù hợp

Tình hình đề kháng kháng sinh của H. pylori tại miền Nam
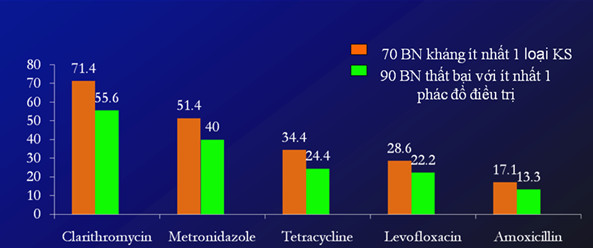 Kết luận
Kết luận
Phát hiện Helicobacter pylori và vai trò sinh bệnh của nó trong loét dạ dày tá tràng là một tiến bộ bước ngoặt của khoa tiêu hoá trong 20 năm gần đây. Những hiểu biết này đồng thời đã làm thay đổi hoàn toàn nguyên lý điều trị: từ việc chỉ trung hoà acid, việc điều trị loét đồng nghĩa với tiệt trừ vi trùng bằng kháng sinh. Tuy nhiên, so với những kết quả lạc quan ban đầu, tỷ lệ tiệt trừ thành công vi trùng đã nhanh chóng sút giảm vì tình hình kháng thuốc đã xuất hiện rất nhanh. Trong điều trị sử dụng kháng sinh bừa bãi, tràn lan và không đúng liều lượng như ở Việt Nam, tỷ lệ kháng thuốc ngày càng nghiêm trọng và dẫn đến tỷ lệ thất bại không nhỏ. Việc khảo sát và ứng dụng những cách điều trị mới bên cạnh kháng sinh thông qua cơ chế miễn dịch như kháng thể IgY, hoặc phát triển một vaccine ngừa H. pylori là hoàn toàn cần thiết cho tình hình hiện tại và tương lai.
Tài liệu tham khảo
Tiếng Việt
- Phan Thị Minh Hương, Hoàng Trọng Thảng (2007). Nghiên cứu hiệu quả liệu pháp kết hợp Esomeprazole + Clarithromycine + Amoxicillin trong điều trị loét dạ dày-tá tràng có nhiễm Helicobacter pylori. Tạp chí Khoa học Tiêu hóa Việt Nam, 5:279-283
- Nguyễn Khánh Trạch, Trần Kiều Miên, Lê Thành Lý (2003). Đánh giá hiệu quả của một tuần điều trị kết hợp Nexium (Esomeprazole), Clarithromycine và Amoxicillin trong diệt trừ Helicobacter pylori và loét tá tràng. Nội khoa, 4:24-32
- Trần Thiện Trung, Đỗ Trọng Hải, Quách Trọng Đức, Lý Kim Hương (2009). Hiệu quả của phác đồ đầu tay EAC và EAL trong triệt trừ H. Pylori. Y Hoc TP. Ho Chi Minh * Vol. 13 – Supplement of No 1 – 2009: 5 – 10.
Tiếng Anh
- Assem M, Efficacy and safety of Levofloxacine, Clarithromycine and Esomeprazol as first line triple therapy for Helicobacter pylori eradication in Middle East, Hepatology Departerment, Egypt.
- Adachi, K., Katsube, T., Kawamura, A., Takashima, T., Yuki, M., Amano, K., Ishihara, S., Fukuda, R., Watanabe, M., and Kinoshita, Y.: CYP2C19 genotype status and intragastric pH during dosing with lansoprazole or rabeprazole. Aliment. Pharmacol. Ther., 14, 1259–1266, 2000.
- Buzas GM,First-line eradication of Helicobacter pylori: are the standard triple therapies obsolete? ,Eur j gastroenterol Hepatol, 2010 May,22(5):597-601
- Furuta, T., Shirai, N., Takashima, M., Xiao, F., Hanai, H., Sugimura, H., Ohashi, K., Ishizaki, T., and Kaneko, E.: Effect of genotypic differences in CYP2C19 on cure rates for Helicobacter pylori infection by triple therapy with a proton pump inhibitor, amoxicillin, and clarithromycine. Clin. Pharmacol. Ther., 69, 158–168, 2001.
- Jafri, NS, Hornung, CA, Howden, CW. Meta-analysis: sequential therapy appears superior to standard therapy for Helicobacter pylori infection in patients naive to treatment. Ann Intern Med 2008; 148:923.
- Peter ,Bismuth improves PPI-based triple therapy for H. pylori eradication, Dis.2010 Oct;11(5):313-8C
- Graham DY, Helicobacter pylori treatment in the era of increasing antibiotic resistance, USA.
- Kuo CH, Rabeprazole can overcome the impact of CYP2C19 polymorphism on quadruple therapy, Taiwan, 2010 Aug , 15(4):265-72
- Makoto Sasaki and et al,Changes in 12-Year First-Line Eradication Rate of Helicobacter pylori Based on Triple Therapy with Proton Pump Inhibitor, Amoxicillin and Clarithromycine, Published online 2010 June 17, Japan.
- Molina-infante J,Clarithromycine vs Levofloxacine in first line triple and sequential regimens for H pylori eradation, Spain, 2010 Aug:32(3):506-7
- Pan X, LiY et al, Efficacy and tolerability of first-line triple therapy with levofloxacine and amoxicillin plus esomeprazole or rabeprazole for the eradication of Helicobacter pylori infection and the effect of CYP2C19 genotype: a 1-week, randomized, open-label study in chinese adults; Clin Ther. 2010 Nov;32(12):2003-11.
- Pontone S, Efficacy of H.pylori eradication with a sequential regimen followed by rescue therapy in clinical practical , 2010, Aug, 42(8):541-3,Italy
- Rokkas T, Sechopoulos P,Cumulative H. pylori eradication rates in clinical practice by adopting first and second-line regimens proposed by the Maastricht III consensus and a third-line empirical regimen., Am J Gastroenterol. 2009 Jan;104(1):21-5.
- Sun Q and et all,High efficacy of 14 –day triple therapy –based, bismuth-containing quadruple therapy for initial Helicobacter pylori eradication, China, 2010 Jun,15(3):233-8
- Sugimoto, M., Furuta, T., Shirai, N., Kodaira, C., Nishino, M., Ikuma, M., Ishizaki, T., and Hishida, A.: Evidence that the degree and duration of acid suppression are related to Helicobacter pylori eradication by triple therapy. Helicobacter, 12, 317–323, 2007.
- Shirai, N., Furuta, T., Moriyama, Y., Okochi, H., Kobayashi, K., Takashima, M., Xiao, F., Kosuge, K., Nakagawa, K., Hanai, H., Chiba, K., Ohashi, K., and Ishizaki, T.: Effects of CYP2C19 genotypic differences in the metabolism of omeprazole and rabeprazole on intragastric pH. Aliment. Pharmacol. Ther., 15, 1929–1937, 2001.
- Vaira D, Zullo A, Vakil N, et al. Sequential therapy versus standard triple-drug therapy for Helicobacter pylori eradication: a randomized trial. Ann Intern Med 2007; 146:556.
- Zhang L,The effect of cytochrome P2C19 and interleukin-1 polymorphisms on H. pylori eradication rate of 1-week triple therapy with omeprazole or rabeprazole, amoxycillin and clarithromycine in Chinese people, Department of Gastroenterology, 2010 Dec;35(6):713-22.
- Zullo, A, De, Francesco V, Hassan, C, et al. The sequential therapy regimen for Helicobacter pylori eradication: a pooled-data analysis. Gut 2007; 56:1353.
- Zhao, F., Wang, J., Yang, Y., Wang, X., Shi, R., Xu, Z., Huang, Z., and Zhang, G.: Effect of CYP2C19 genetic polymorphisms on the efficacy of proton pump inhibitor-based triple therapy for Helicobacter pylori eradication: a meta-analysis. Helicobacter, 13, 532–541, 2008.
[1] ThS. BS. Lê Đình Phương, Trưởng khoa Nội Tổng quát và Y học Gia đình, Bệnh viện FV
THÔNG TIN HỮU ÍCH

- Các phương pháp xét nghiệm vi khuẩn Hp chính xác nhất
- Diệt Hp sớm để phòng ngừa ung thư dạ dày
- Phác đồ điều trị đau dạ dày do vi khuẩn Hp
- Bố mẹ bị nhiễm vi khuẩn Hp làm sao phòng bệnh cho con?
Tin mới nhất
-
 Thoái hóa điểm vàng thể ướt
Thoái hóa điểm vàng thể ướt
- Nấm lim xanh giá bao nhiêu tiền 1kg mua nấm lim xanh ở đâu là tốt?
- Áp xe quanh hậu môn
- Top Điều Cần Biết Về Đông Trùng Hạ Thảo Tây Tạng
- Viễn Chí và tác dụng chữa bệnh của Viễn Chí
- Ngộ độc rượu
- Uống nấm lim xanh có tốt không cách uống nấm lim rừng hiệu quả
- Danh sách các bác sĩ chữa liệt dương giỏi nhất tại Hà Nội và Hồ Chí Minh
- Thuốc bổ sung canxi Calcium Corbiere: Công dụng, cách dùng và lưu ý
- Nội soi mật tụy ngược dòng (ERCP)